光合成という植物の基本能力を捨て、菌類ネットワークに「ただ乗り」する菌従属栄養植物(マイコトロフ)。一見すると怠け者に見えるかもしれませんが、実はこの選択は極限の環境への究極の適応戦略です。
地下に張り巡らされた見えない菌類ネットワークを巧みに操り、樹木から間接的に養分を奪う仕組みは、生命の多様性と創意工夫に満ちています。光合成をやめた植物たちが選んだ共生戦略から、自然界の普段私たちの目には見えない場所にある世界を垣間見ることができます。

寄生でもなく、共生と言えるのか複雑な存在、菌従属栄養植物…。その不思議で巧みな生態を見ていきましょう!


「菌従属栄養植物」とは ― 菌類のネットワークに頼る生き方


出典:WIKIMEDIA COMMONS – Pink indian pipes
森の静かな地面の下には、私たちの目には見えない、驚くほど複雑な菌類のネットワーク(菌糸ネットワーク)が広がっています。そこに生きる菌従属栄養植物(マイコトロフ mycoheterotroph )は、植物の基本ともいえる光合成を手放し、菌類との特別な関係に命を託すという独特な道を選びました。
このような選択をした植物たちは、見た目や生態が通常の植物とは大きく異なり、その生き方は生命の多様性の中でも個性が際立つ存在といえます。
菌糸ネットワーク(菌根菌ネットワーク)🕸️🍄
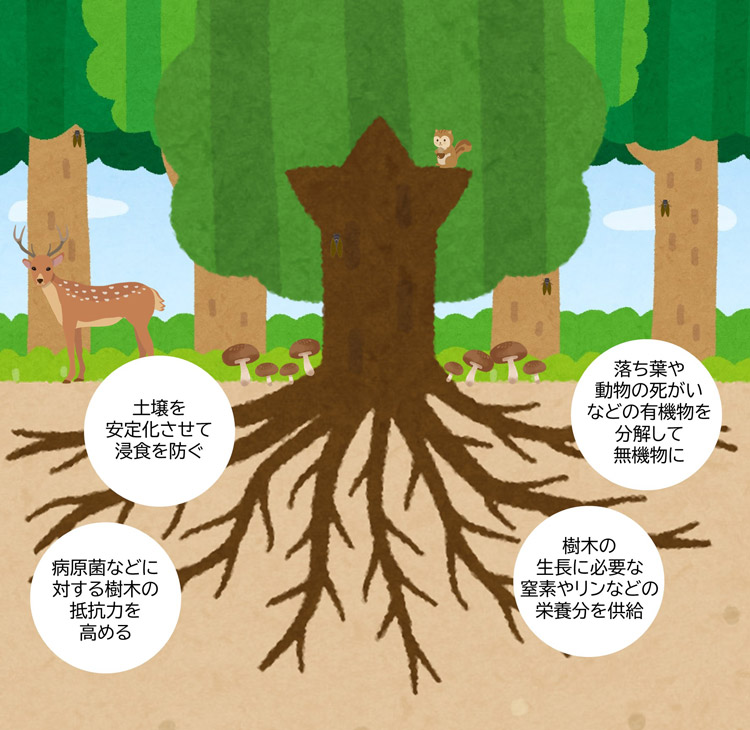
森の地面の下には、きのこやカビの仲間が作る「菌糸(きんし)」という細い糸が、まるで見えないクモの巣のように広がっています。この菌糸どうしはお互いにつながり合い、多くの木や草の根と結びつきます。その仕組みを「菌根菌ネットワーク」または「ウッドワイドウェブ」と呼びます。
菌類は土の中の栄養分や水分を集めて植物に送り、植物はそのお返しに自分が作った栄養(ブドウ糖など)を菌類に渡します。菌糸を通じて、木どうしや違う植物どうしが、お互いに栄養や情報をやりとりしたり、病気の木に力を貸したりすることもあることがわかってきました。



植物も種を超えた助け合いをすることがあるのですね!
このような地下のネットワークは森の健康や生物の多様性を支える大切なしくみです。

出典:JSTサイエンスポータル – 森林生態系を支える菌根菌ネットワーク
参考・引用



この不思議な植物の正体を理解するため、まずは
基本的な定義
長く続いた誤解の歴史
混同されやすい他の植物との違い
を整理しておきましょう。
菌従属栄養植物の定義 ― 光合成をやめて「菌類」に頼る植物たち
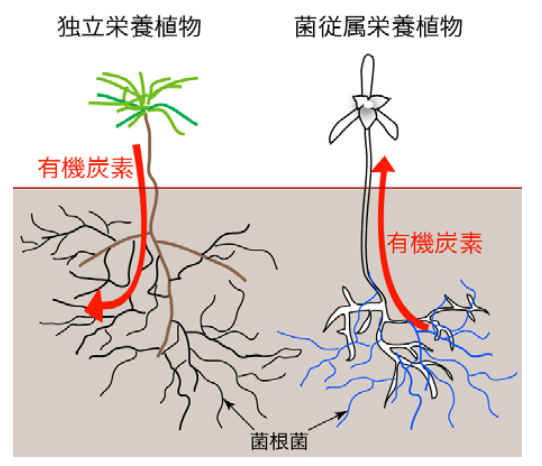
菌従属栄養植物とは、光合成によって自ら栄養を作り出すことをやめ、生きるために必要な栄養のすべて、あるいは一部を菌類から得ている植物のことです。通常の植物が太陽光と二酸化炭素を使ってエネルギーを生み出すのに対し、これらの植物は菌根(mycorrhiza)という、根と菌類が一体となった器官を通じて、菌類が吸収した栄養を間接的に受け取っています。

出典:植物科学最前線 ‐ 菌従属栄養植物の系統と進化 遊川 知久(2014年)
菌従属栄養には、その程度によって異なるタイプが存在します。
完全菌従属栄養植物
最も完全な形が「完全菌従属栄養植物」で、光合成をまったく行わず、葉緑素も持たないため、白色や淡黄色、ときに赤紫色など、多くの場合緑色以外の姿をしています。
ギンリョウソウ(Monotropastrum humile )はその代表例で、地上に姿を現すのは花を咲かせるわずかな期間だけです。


出典:iNaturalist – ギンリョウソウ Monotropastrum humile
部分的菌従属栄養植物
一方、「部分的菌従属栄養植物」は光合成と菌類依存の両方を行い、光の少ない環境では菌類からの栄養補給に頼りながら、光が十分にある環境では自分の光合成も活用するという柔軟な戦略を取っています。
これらの植物が存在することは、地下に存在する菌根システムが多くの植物にとっていかに重要であるかを示しています。実は、完全菌従属栄養であると考えられていた植物でも、花や果実をつくる時期だけは光合成を行うものもあることが最近の研究で明らかになっており、菌従属栄養性の定義は思った以上に複雑です。
「腐生植物」という歴史的な誤解 ― なぜ「腐生」ではないのか
かつて、これらの植物は「腐生植物(saprophyte)」と呼ばれていました。この名称は、植物自身が枯れ葉や倒木などの有機物を直接分解して栄養を得ていると考えられていたことに由来します。科学がまだ発展途上だった時代、研究者たちは「光合成をしないなら、有機物を直接食べているのだろう」という素朴な推理をしたのです。
しかし、その後の研究によって、植物には動物や真菌が持つような、有機物を分解するための強力な酵素系がないことが明らかになりました。実際に落ち葉や倒木を分解しているのは菌類であり、菌従属栄養植物はその菌類に接続し、間接的に栄養を得ているのです。


出典:神戸大学 ‐ 枯れ木を食べる植物「腐生植物」は存在するのか!?(2020年1月24日)
この誤解を決定づけるターニングポイントは、1990年代後半から普及し始めた安定同位体解析※という技術でした。この手法により、光合成をしない植物の体に含まれる炭素が、地表の有機物ではなく、菌類を介して他の樹木から供給されていることが科学的に証明されたのです。
安定同位体解析🧪📊
自然界に存在する炭素や窒素などの元素には、原子番号は同じでも質量がわずかに異なる「安定同位体」という兄弟のような存在があります。例えば炭素では、通常の¹²Cより少し重い¹³Cが、窒素では通常の¹⁴Nより重い¹⁵Nが一定の比率で自然界に存在しています。
安定同位体解析とは、生物の組織内に含まれるこれらの「重い同位体」と「軽い同位体」の比率(δ¹³Cやδ¹⁵N値と表記)を超高精度の質量分析計で測定し、その生物の栄養源を追跡する手法です。
この手法が優れているのは、生物が栄養を摂取する際に「同位体分別」という現象が起きるためです。具体的には、光合成をする植物はRuBisCOという酵素を使ってCO₂を固定する過程で、軽い¹²Cを好んで取り込み、¹³Cは相対的に少なく取り込みます。
この「選別のクセ」は、生物ごと、過程ごとに異なるため、組織に蓄積した同位体の比率は、その生物が「何から栄養を得たか、どのような栄養摂取経路を辿ったか」を示す、いわば「食生活と栄養摂取の痕跡」となるのです。


出典:京都大学 ‐ 安定同位体生態学の簡単な解説
例えば、光合成をしない菌従属栄養植物の組織から測定される¹³C値や¹⁵N値が、地表の腐葉土のパターンではなく、むしろ菌類や菌類の先にある樹木のシグナルと一致することが科学的に証明されました。従来の観察眼だけでは決してわからなかった、地下に広がる「見えない栄養の流れ」を、同位体という「目に見えない指紋」によって可視化することに成功したのです。
他にも以下のような、安定同位体解析により、それまでの定説が覆された事例はあります。
1. アサリの食性:陸由来有機物 → 海洋植物プランクトン選択
干潟のアサリは豊富な陸由来有機物を主食としているという通説に対し、δ¹³C分析により、実際には海洋植物プランクトンを選択的に摂食していることが判明しました。
2. 菌従属栄養植物の栄養源:腐葉土分解 → 菌類ネットワーク経由の樹木依存
100年以上「腐生植物」と呼ばれ、腐葉土を直接分解していると信じられていた光合成をしない植物が、実際には菌類を介して生きた樹木から栄養を得ていることが証明されました。
3. ネアンデルタール人の食性:雑食・魚食説 → 大型草食獣の肉食専門
高いδ¹⁵N値から淡水魚や雑食と解釈されていたネアンデルタール人の食性が、アミノ酸別同位体解析により、実際には大型草食動物の肉を主食とする頂点捕食者であったことが判明しました。
4. 菌根ネットワークの役割:二者間共生 → 複数樹木間の双方向炭素移動
菌根共生は「植物と菌類の一対一の関係」と考えられていましたが、安定同位体トレーサーにより、複数の樹木が菌糸ネットワークでつながり、季節によって炭素の流れる方向が変化する動的システムであることが明らかになりました。
5. 窒素循環:死後の土壌分解経由 → 生きた菌根ネットワーク経由の直接移行
マメ科植物が固定した窒素は死後に土壌を通じて他の植物に供給されると考えられていましたが、δ¹⁵N分析により、生きている間に菌根ネットワークを通じて直接他の植物へ移動していることが証明されました。
6. 食物網構造:直線的階層モデル → 複雑な非線形ネットワーク
栄養段階ごとにδ¹⁵N値が一定の割合で増加する「階層的食物連鎖」モデルが標準とされていましたが、多様な生態系での同位体解析により、実際の栄養移行はより複雑で非線形的であることが判明しました。
参考・引用
Wiley Online Library – 15N and 13C natural abundance of two mycoheterotrophic orchids
日本生態学会 – 琵琶瀬川河口干潟産のアサリの安定同位体比分析
Max Planck Institute – Neandertals’ main food source was definitely meat
Nature Plants – Mycoheterotrophy in the wood-wide web
Wikipedia – Mycorrhizal network
水産総合研究センター – 貝塚出土アサリ貝殻の安定同位体比からみえること
PNAS – Isotopic evidence for the diets of European Neanderthals
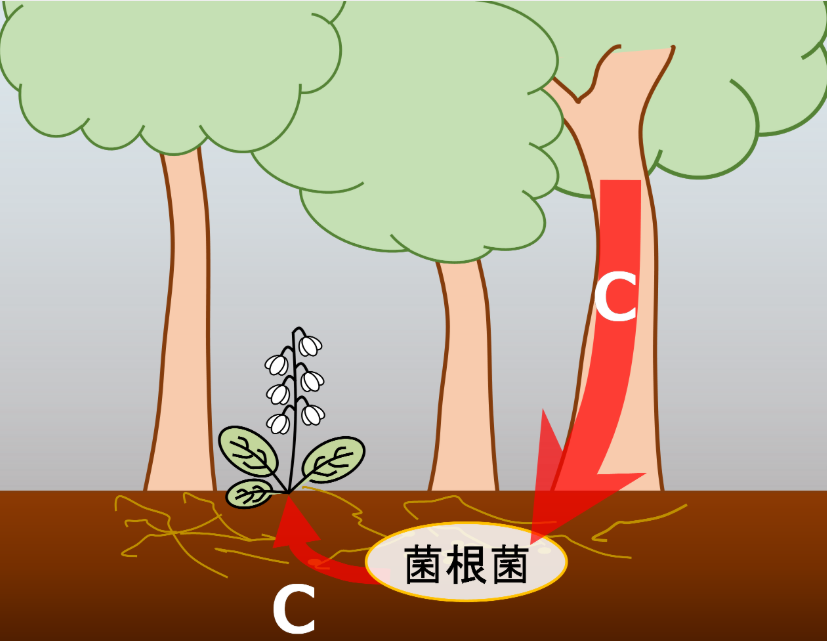

出典:山形大学 ‐ 林床植物は共生する菌類にも炭素源を依存しているか? 近年海外で発表された見解の再検証(2022年3月22日)
現在では、「腐生植物」という用語は誤解を招くものとして徐々に使われなくなり、より正確に栄養摂取の仕組みを表す「菌従属栄養植物」という呼び名が定着しつつあります。ただし、実際には一部の菌従属栄養植物は木材を分解する腐朽菌に依存しており、菌糸のネットワークを通じて数十年前に固定された「古い炭素」を利用していることも明らかになっています。



この意味では、間接的ながら「腐生」という側面も持っていると考えることもできますね。
「寄生植物」との決定的な違い ― 直接奪うか、間接的に頼るか
菌従属栄養植物と混同されることが多いのが「寄生植物(parasitic plant)」です。どちらも他の生物から栄養を得るという点では共通していますが、そのメカニズムは根本的に異なります。
寄生植物は「吸器」と呼ばれる特殊な器官を使って、他の植物の茎や根に直接取り付き、宿主の維管束※に接続して、水分や養分を物理的に吸い取ります。ネナシカズラやラフレシア、日本ではヤドリギなどが代表例で、これらは養分を得るために宿主植物に直接付着しており、宿主は大きな負担を強いられます。
維管束(いかんそく)🌿💧
維管束(いかんそく)は、植物の根や茎、葉に通っている、水や栄養分を運ぶための「パイプ」のような組織です。維管束は「道管(どうかん)」と「師管(しかん)」という二つの細い管からなっており、道管は根から吸い上げた水と土の中の栄養を上へ運び、師管は葉で作られた栄養分を下へ運びます。
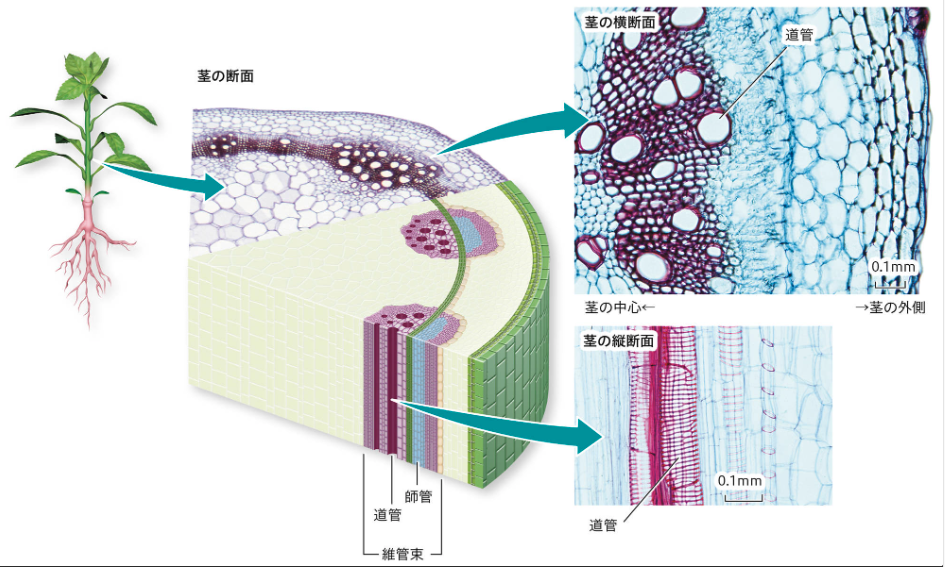

出典:学校図書 ‐ 道管と師管
これら多数の道管と師管が集まった部分を、それぞれ「木部(もくぶ)」「師部(しぶ)」と呼びます。茎の断面を観察すると、維管束が小さな穴(道管)として見えることがあり、茎を太らせるために木部と師部の間には「形成層(けいせいそう)」という細胞分裂の活発な層が存在します。
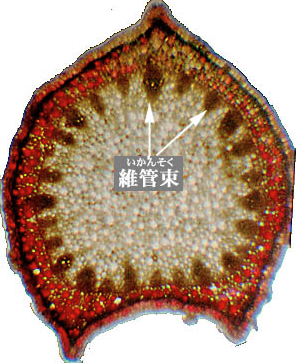

出典:神戸大学 ‐ 専門的な言葉の詳しい解説 維管束 いかんそく
また、葉では維管束が筋状に走っており、これが「葉脈(ようみゃく)」として目に見える構造です。植物全体に水と栄養を効率よく届けるため、欠かせない組織です。


出典:WIKIMEDIA COMMONS – Starr 041211-1365 Unknown pteridophyte
参考・引用


出典:iNatiralist – ヤドリギ Viscum album
これに対し、菌従属栄養植物は他の植物に直接触れることはなく、菌類という「仲介者」を介して栄養を得ています。菌根菌は樹木とも関係を持っており、同じ一本の菌糸体が複数の植物と共生することもあります。
つまり、菌従属栄養植物は単一の植物から直接栄養を「吸収」するのではなく、菌根ネットワーク全体の中から間接的に栄養を「受け取る」という、より複雑で巧妙な仕組みになっているのです。
また、寄生植物には半寄生植物(光合成も行う)と全寄生植物(光合成をしない)という分類がありますが、この分類基準は「光合成を行うか否か」です。一方、菌従属栄養植物の分類基準は「菌類への依存度」であり、同じ菌従属栄養植物でも光合成能力の有無という点では異なります。
このように、両者は栄養摂取の仕組みだけでなく、分類の基準そのものが異なっているのです。
寄生植物に興味がある人には、こちらもおすすめ👇️
菌従属栄養植物は、植物でありながら光合成を捨て、菌類ネットワークという見えない世界に生きる道を選びました。長い間「腐生植物」と誤解され、寄生植物とも混同されてきましたが、現代の科学技術がその真の姿を明らかにしつつあります。
このような植物の存在は、森の地下に広がる豊かな菌類ネットワークの証であり、生命がいかに多様な戦略で環境に適応しているかを静かに教えてくれるのです。


菌従属栄養植物 研究の歩み ― 謎に満ちた生態の解明史


出典:神戸大学:約1世紀ぶりの快挙! 新属新種の植物「ムジナノショクダイ」を発見(2024年3月1日)
※約100年ぶりにタヌキノショクダイ科の新属新種が発見された快挙
森の暗い林床に現れる、光合成をしない白い幽霊のような植物。菌従属栄養植物は、長く「謎の存在」として扱われてきました。その不思議な生態は、古くから植物学者たちを魅了し続けてきましたが、地下の見えない世界で何が起きているのかを解明するには、科学技術の進歩を待つ必要がありました。
その研究史は、実は「見えないものを見る」ための、一世紀以上にわたる壮大な挑戦の記録なのです。時代ごとの転換点を追っていきましょう。
18~19世紀 ― 「奇妙な腐生植物」として分類された時代
この時代、植物学者たちは森の暗い林床に咲く、葉緑素を持たない植物に気づき始めました。当時の常識であった「植物は光合成をする」からあまりにもかけ離れていたため、これらの植物は枯れ葉や倒木を直接分解する「腐生植物」として広く信じられていました。
そのような風潮の中、1881年ポーランドの植物学者カミエンスキー※は、ギンリョウソウが周辺の樹木と菌類を共有し、菌糸を通じて栄養を得ているという革新的な仮説を提唱しました。しかし「花を咲かせる植物が菌から栄養を奪う」という概念は当時受け入れがたく、この仮説は長く埋もれてしまったのです。



あまりに革新的な発想に、周囲はついていけなかったのですね
※Franciszek Dionizy Kamieński(フランチェシェク・ディオニジ・カミエンスキー):専門は寄生植物


出典:WIKIMEDIA COMMONS – Franciszek Kamieński
20世紀後半 ― 転換点となった「安定同位体解析」の登場
カミエンスキーの仮説が科学的に検証される転機は1960年に訪れました。スウェーデンの森林生態学者ビョークマン(Erik Björkman)が、放射性同位体(¹⁴C標識グルコースと³²Pリン酸塩)を樹木に注入し、わずか5日以内にギンリョウソウの組織に転移することを実証したのです。カミエンスキーの80年前の仮説が、ついに科学的に証明された瞬間でした。
放射性同位体(ラジオアイソトープ)⚛️
自然界の原子の中には、エネルギー的に不安定な状態にあり、安定しようとして「放射線」というシグナルを出すものがあります。これを放射性同位体と呼びます。生態学では、この性質を、物質の動きを追跡するための「発信機付きのタグ(トレーサー)」として利用します。
【放射性同位体がトレーサーになるまでの歩み】
- 1896年 アンリ・ベクレル、放射能を発見:ウラン塩が自発的に「見えない線(放射線)」を放つことを見つけ、放射能研究が始まる。
- 1900〜1913年 ラザフォードとフレデリック・ソディ、原子核変換と同位体概念を確立:放射性崩壊の仕組みを明らかにし、同じ元素でも質量が異なる「同位体」という基本概念を提示する。
- 1923年 ゲオルク・ヘヴェシー、放射性同位体を“トレーサー”として初めて本格的に利用:植物や動物の体内で物質がどのように移動するかを放射性同位体で追跡する方法を確立し、後の生物学研究の礎になる。
- 1940〜1950年代 多分野で放射性トレーサー法が普及:医学・農学・生態学などで栄養塩、水、薬物などの“目に見えない動き”を測定する標準的手法として広まる。
- 1960年代 森林生態学・菌従属栄養植物研究に応用が拡大:地下の菌根ネットワークを直接証明するための強力な手段として、放射性同位体が活用され始める。
- 現在 放射性同位体に加え、安定同位体(¹³C、¹⁵Nなど)も主流に:高感度分析技術の向上により、より安全で精密な物質循環研究が可能に。生態系の“見えない流れ”を描き出す不可欠なツールとなる。
1960年、スウェーデンの森林生態学者エリク・ビョークマンは、こうして発展してきた放射性トレーサー法を菌従属栄養植物の研究に本格的に導入しました。彼は炭素(¹⁴C)で標識したグルコースやリン(³²P)を樹木に与え、その放射性シグナルが菌根菌を経由してギンリョウソウへと移動していく様子を精密に追跡しました。
わずか数日で樹木 → 菌類 → ギンリョウソウへと流れる経路が検出され、地下の栄養移動が単なる仮説ではなく、明確な証拠を伴う事実として示されたのです。この研究は、普段は完全に目に見えない地下ネットワークの存在を、放射性同位体という科学的ツールによって地図として描き出した、現代生態学を象徴する成果のひとつと言えます。
参考・引用
New Phytologist Foundation ‐ Mycoheterotrophy: The biology of plants living on fungi (2009)
1990年代以降、安定同位体解析(δ¹³C、δ¹⁵N)が普及すると、菌従属栄養植物の組織が腐葉土ではなく、菌類や樹木のシグナルと一致することが次々と確認され、100年以上続いた「腐生植物」という誤解が完全に解消されました。
21世紀~現在 ― ゲノム科学が解き明かした菌類ネットワークとの共生
21世紀、次世代シーケンサー※の普及により、菌従属栄養植物のゲノム解析が可能になると、その進化のメカニズムが明らかになってきました。光合成をやめた植物の葉緑体ゲノムは通常の150kbから極端な場合20kb以下にまで縮小し、光合成遺伝子が系統ごとに独立して複数回失われていることが判明したのです。
※次世代シーケンサー:DNA配列を従来の方法よりも圧倒的に高速・大量・低コストで読み解く装置
2022年、ラン科の比較ゲノム研究では、部分的菌従属栄養と完全菌従属栄養が段階的に進化し、光受容体遺伝子やオーキシン※輸送体遺伝子が段階的に削除されていることが示されました。この「収束進化」※は、光合成をやめることが複数の系統で何度も最適な適応戦略として「再発明」されたことを意味しています。
※オーキシン:植物の成長、発育、屈性(光や重力への応答)を制御する重要な植物ホルモン



この結果、ラン科ネッタイ亜族を代表として、ギンリョウソウ属など複数の系統で以下のようなことが起こりました。
光への応答能力の喪失
根の形態と方向性の変化
葉と根の構造の退化・消失
成長パターンの変化(幼生状態のまま成熟)
収斂進化🦉🦇
収斂進化(しゅうれんしんか)とは、まったく異なる進化の道をたどった生き物が、似たような環境に適応するため、結果的に似たような姿や能力を獲得することです。たとえば、海のイルカ🐬(哺乳類)と魚のサメ🦈(魚類)は、遠い親戚ですが、水中を速く泳ぐために流線型の体とヒレを獲得しました。
空を飛ぶコウモリ🦇(哺乳類)と鳥🕊️(鳥類)も、同じように羽を広げて飛び立ちます。これは、限られた環境で生き残るために、最も効率の良い形や能力が、偶然にも「収束」した結果なのです。


出典:Wikipedia『収斂進化』
例えば、モグラ(哺乳類)とケラ(昆虫)は、どちらも土を掘って暮らす「地中生活者」です。そのため、モグラの前脚とケラの前脚は、土をかき出すために幅広く平たい形状になった点で収斂進化しています。
菌従属栄養植物の研究は、19世紀の観察から始まり、20世紀の同位体トレーサー技術を経て、21世紀のゲノム科学へと発展してきました。かつて「奇妙な腐生植物」として片付けられていましたが、実は菌類ネットワークに高度に適応した生き方であること、そしてその進化が複数系統で独立して起きていることが判明したのです。


なぜ「菌類依存」という道を選んだのか? ― 進化の背景


出典:MEXICO AMBIENTAL ‐ Lacandonia schismática, flor endémica de México(2018年12月21日)
※雄しべと雌しべの位置が逆という、世界でも類を見ない奇妙な花の構造
植物の命綱ともいえる「光合成」を、なぜ菌従属栄養植物はあえて手放すという大胆な道を選んだのでしょうか。一見すると「退化」のように思えるかもしれませんが、これは厳しい自然界を生き抜くための、驚くほど合理的で巧みな「適応戦略」なのです。
光合成のコストと「暗い林床」という生存ニッチ
光合成は「無料」で行えるわけではありません。葉緑体やその関連タンパク質を製造・維持管理するには、膨大なエネルギーと資源投資が必要です。特に、森の林床のような光が極端に少ない環境では、この「投資」が報われにくいのです。
実際、特に暗い落葉樹林の林床では、地表に到達する光は全日射の約1~10%程度であり、深い常緑樹林ではさらに低く0.5~2%程度の場所も存在します。このような極限の暗さでは、光合成に必要な光受容体やクロロフィルを維持するコストが、光合成により得られる炭素よりも大きくなる可能性が高いのです。



森の暗い場所では、光合成装置を維持するとエネルギー収支が「赤字経営」になってしまうのです。
一方、菌根菌との共生関係がすでに確立されている植物にとって、菌類から直接栄養を得る方が、光合成装置を維持・稼働させるよりもコストパフォーマンスが高い場合があります。このような条件下では、「暗い林床」という競争相手の少ない「ニッチ」※で生き残るため、光合成を段階的に、そして最終的には完全に手放す戦略が有利になったのです。
ニッチ(Niche)🎯🧩
ニッチ(niche)という言葉は、もともとフランス語で「壁のくぼみ」や「装飾用の小さな空間」を意味する建築用語でした。1917年、生態学者ジョセフ・グリニル(Joseph Grinnell)は、この比喩的な表現を使って、特定の生物が生態系の中で占める独特な「位置」や「役割」を説明するようになりました。
つまり、現代における「ニッチ」とは、ある生物が「何を食べるか」「どこに住むか」「いつ活動するか」など、その生物が利用できる環境条件・資源の総合的なパターンのことです。建築物の「壁のくぼみ」のように、生態系においても、各生物は「独自のくぼみ」を占めており、その中で他の生物と競合しないで生存しているのです。
-1024.png)
-1024.png)
出典:GeeksforGeeks – Ecological Niche
特に興味深い点は、同じ環境内で複数の生物が共存するために、それぞれが微妙に異なる「ニッチ」を利用している、ということです。例えば、光合成をする植物が優占する明るい環境では、菌従属栄養植物は「光が極めて少ない林床」というニッチを独占的に利用することで、競争を回避し、生存しているのです。このようなニッチの多様性が、生態系の豊かさと安定性を支えています。
Wikipedia ‐ ニッチ
People and Nature (Journal) – The socio‐ecological niche(2025年4月)
EcoEvoRxiv – Re-revisiting the Niche Concept (Leibold, 2025年)
菌根共生から一方的搾取へ ― 「助け合い」が「ただ乗り」に変わる進化
光合成をやめる進化は、突然始まったわけではありません。多くの植物は、地下で菌類と「菌根(mycorrhiza)」を結び、植物は光合成産物を菌に提供し、菌は土壌からの栄養を植物に供給するという共生の関係を築いています。
しかし、この共生関係には本質的な脆弱性があります。特にアーバスキュラー菌根菌(arbuscular mycorrhizal fungi)が形成する菌糸ネットワークは、複数の植物と同時に共生するため、一部の植物が光合成産物を提供しなくても、他の植物からの供給で菌類は生存できるのです。
進化生物学では、このような相利共生における「チーター(cheater)」…相手に利益を与えずに自分だけ利益を得る個体が進化することが理論的に予測されています。菌従属栄養植物は、まさにこのチート戦略が進化的に成功した例なのです。



この「フリーライド(ただ乗り)」戦略は、相手かまわず行うのではなく、特定の菌類だけに狙いを定めることで成功してきました。
もし手当たり次第にただ乗りしようとすれば、菌類側に対策されて関係を断たれてしまうかもしれません。しかし、特定の菌類とだけ深く関わる(高い特異性を持つ)ことで、相手のシステムに巧みに入り込み、数百万年もの間、関係を維持できるように進化したのです(2008年の研究より)。
つまり、菌従属栄養植物は単なる「フリーライダー」ではなく、高度に特化した「ニッチ専業者」として進化したわけです。
還元進化 ― 失われた光合成遺伝子と極限のゲノム縮小
光合成をやめると決まれば、光合成に必要な遺伝子は不要になります。生物進化では、機能しなくなった遺伝子を維持することもまた「コスト」であり、このコストを削減するために遺伝子は次々と失われていきます。この現象を「還元進化」※と呼びます。
還元進化(reductive evolution)📉
還元進化(かんげんしんか)は、生物が進化の過程で、特定の器官や遺伝子、機能などを失い、よりシンプルな体つきになることです。これは、効率を追求してエネルギーコストを節約する、積極的で合理的な「適応」戦略の一つです。
代表的な例として、光のない洞窟に住む魚(ブラインドケーブ・カラシン)が目を失う代わりに他の感覚を発達させたり、宿主の栄養に頼る寄生動物(サナダムシなど)が自らの消化管を失ったりしています。全寄生植物が光合成の遺伝子を失うのも、この還元進化の顕著な例です。


出典:WIKIMEDIA COMMONS – Astyanax jordani SeaDonuts1
微生物の世界ではさらに極端な例が見られます。アブラムシの体内に共生する細菌ブフネラ(Buchnera aphidicola)は、自由生活から共生生活へ移行する際に、遺伝子を元の約4分の1(約56万塩基対)にまで縮小させました。これにより、膨大なエネルギーを節約できますが、同時に柔軟性が失われ、宿主なしでは生きられなくなります。
人間にも還元進化の痕跡があります。尾てい骨(尾椎骨、コッキックス)や虫垂(ちゅうすい)は、かつて祖先ではより大きな機能を持っていました。クジラの骨盤も、陸上の祖先が持っていた後ろ脚の名残で、現在では生殖に関連する筋肉の付着点として限定的な機能を持つだけです。
還元進化は、不要なコストを削減できるメリットがある一方、環境変化への対応力(柔軟性)が失われるデメリットもあります。
⚠️ 「退化」との違いと用語の注意点
「退化」という言葉は、しばしば「劣るようになった」という否定的な(価値判断の)意味合いで使われます。しかし、生物の進化に「優劣」はありません。
還元進化は、環境に適応した結果として機能を失う合理的な「変化」です。そのため、科学の世界では価値判断を含まない「還元進化」や「後退進化」という言葉を使うことが推奨されます。また、「痕跡器官(vestigial organ)」は、かつて機能していたが現在は元の機能を失った器官を指し、還元進化の結果として生じたものです。
参考・引用
吉田 聡子, 白須 賢 ‐ ストライガのゲノム解析から見えてきた寄生植物の進化(2020年)
Biology Insights – Buchnera and Aphids: Symbiosis, Genomics, and Co-evolution
Wikipedia – Human vestigiality
The Scientist – What Does the Appendix Do?
PMC (PubMed Central) – A Glimpse Towards the Vestigiality and Fate of Human Appendix
Academia.edu – Reductive Genome Evolution In Buchnera Aphidicola
また、注目すべきは完全に失われた遺伝子もあれば、部分的に保持されているものもあるという点です。例えば、葉から光合成遺伝子が失われた部分的菌従属栄養植物でも、根や茎の一部には痕跡的に光合成関連遺伝子が残存していることがあります。
このような「段階的な遺伝子喪失」は、菌従属栄養への進化が一度に起きたのではなく、徐々に光合成への依存を減らしていった過程を如実に物語っています。還元進化は、単なる遺伝子の「削除」ではなく、生存に最低限必要な遺伝子を残しながら不要な部分を効率的に削ぎ落とす、洗練された最適化のプロセスなのです。



このように、菌従属栄養植物は、
①厳しい光環境から逃れ
②すでにある菌類との共生関係を巧みに利用し
③不要な機能を捨てる
という合理的なステップを経て、現在の独特な生き方を確立しました。
驚くべきことに、この進化はたった一度の偶然ではありません。全く異なる種類の植物たちが、それぞれの歴史の中で何度も、この「光合成をやめる」という道を選んできたのです。まるで、暗い森で生き抜くための「正解」として、多くの植物が別々にこのスタイルを再発明したかのようです。
この事実は、生命がいかに柔軟で、したたかな戦略を持っているかを私たちに教えてくれます。


菌従属栄養植物の「戦略」 ― 菌類ネットワークへの侵入から繁栄まで
:focal(353x261:354x262)/https://tf-cmsv2-smithsonianmag-media.s3.amazonaws.com/filer/bc/d2/bcd2f072-a487-4873-9c9c-378b2b41d782/gastrodia-agnicellus.jpg)
:focal(353x261:354x262)/https://tf-cmsv2-smithsonianmag-media.s3.amazonaws.com/filer/bc/d2/bcd2f072-a487-4873-9c9c-378b2b41d782/gastrodia-agnicellus.jpg)
出典:Smithsonian Magazine ‐ Behold the World’s Ugliest Orchid, According to Botanists(2020年12月21日)
※「世界で最も醜いラン」と評され話題に
光合成をやめた菌従属栄養植物は、ただ受動的に養分を待っているだけではありません。彼らは暗い森の地下で生き抜くため、見えない菌類ネットワークに巧みに「侵入」し、特定の菌類パートナーを見極め、複雑なネットワークから栄養を得て、次世代に命をつなぐための驚くほど高度な戦略を持っています。
その巧妙な生存戦略の中でも、特に重要な3つのポイントを見ていきましょう。
1.特定のパートナーを選ぶ「菌類特異性」 ― 菌種を見極める化学センサー
菌従属栄養植物は、土の中にいる菌類なら誰でも良いというわけではありません。数千種もの土壌菌の中から、特定の科や属の菌類だけを「パートナー」として選ぶ、非常に高い「菌類特異性」を持っています。
「適合菌」と呼ばれるこれらのパートナー菌は、特定の化学シグナルを発すると考えられており、菌従属栄養植物はこのシグナルを感知して適合菌を見極めています。2022年の研究では、タケラン属(Gastrodia)の完全菌従属栄養種が、発芽時には腐朽菌Mycena属と共生し、成体では別のキノコ属(Gymnopus属)に切り替わることが明らかになりました。
この「菌類のスイッチング」は単なる柔軟性ではなく、ライフステージごとに最適なパートナーを選別する戦略なのです。


出典:Frontiers in Plant Science ‐ Mycorrhizal Switching and the Role of Fungal Abundance in Seed Germination of the Fully Mycoheterotrophic Orchid Gastrodia confusoides(2022年1月12日)
※上の写真
(A)竹の落葉の間に生育し、花を咲かせた成植物(スケールバー = 1 cm)
(B)花が受粉に成功した後の茎の伸長(スケールバー = 10 cm)
(C)受粉から2週間後、成熟した果実が開き、種子(矢印)を放出しました。(スケールバー = 1 cm)
(D)腐敗した竹の落葉にある菌根(矢印)のある管(スケールバー = 1 cm)
(E)根の皮質細胞に菌根菌が存在することを示す光学顕微鏡断面。E:表皮細胞、C:皮質細胞、H:菌糸(スケールバー = 10 μm
興味深いことに、この高い特異性は宿主菌類側にも選別圧をかけています。菌類にとって、光合成産物を提供しない「チーター」を受け入れることは本来不利益であるため、菌類は特定の化学物質を発して自分に相応しいパートナーだけを選別する防御機構を進化させました。



つまり、菌従属栄養植物の「選別能力」と菌類の「防御機構」が何百万年にわたって競争・共進化を続けた結果が、現在の高度な特異性なのです。
2.菌類のネットワークから養分を「盗む」メカニズム ― 三者関係の巧妙な構造
菌従属栄養植物の多くは、菌類そのものから養分を奪っているのではなく、菌類が同時に共生している「近くの緑豊かな樹木」が作った栄養を横取りしています。つまり、「樹木(光合成産物の供給源)→菌根菌(仲介役)→菌従属栄養植物(受取手)」という三者関係のネットワークに、巧みに「割り込む」ことで生存しているのです。
樹木は光合成で作った炭素(スクロースなどの糖類)を菌根菌に提供し、菌根菌は土壌から吸収した窒素やリンなどを樹木に返す相利共生を行います。菌根菌の菌糸ネットワークは地下で数メートル以上にわたって広がり、複数の樹木や植物と同時に接続しているため、一部の植物(菌従属栄養植物)が栄養を提供しなくても、他の樹木からの供給で菌類は生存できるのです。
菌従属栄養植物はこのネットワークの「隙間」に侵入し、樹木が何十年にもわたって蓄積した光合成産物を、菌糸を通じて吸収しているのです。また、安定同位体解析により、菌従属栄養植物(特にオニノヤガラなど)が樹木から供給された「新しい炭素」だけでなく、数十年前に固定された「古い炭素」※も利用していることが判明しており、彼らは実に多層的で柔軟にネットワークを利用していることがわかります。



ここで言う「古い炭素」には、例えば以下のようなものがが該当します。
✓ 枯れ木(倒木・朽木)に含まれる炭素
✓ 落ち葉や死んだ枝に含まれる炭素
✓ 分解産物としての「二次的な炭素化合物」
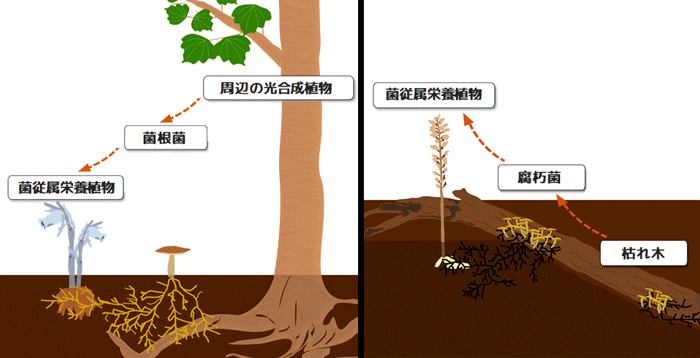

出典:神戸大学 ‐ 枯れ木を食べる植物「腐生植物」は存在するのか!?(2020年1月24日)
3.超微細な「埃種子」と発芽の秘密 ― 菌類なしでは発芽できない運命
菌従属栄養植物の多くは、ラン科植物と同様に「埃種子」と呼ばれる、栄養(胚乳)をほとんど持たない超微細な種子を大量に生産します。大きさは0.05~6mmと極めて小さく、一粒の重さは数マイクログラムにすぎません。


出典:WIKIMEDIA COMMONS – Seeds of Vanda tessellata 2


出典:横浜国立大学学術情報リポジトリ ‐ 横浜国立大学におけるタシロランの分布と生育状況
※(A)花序がついていた塊茎 (B)塊茎を掘りとった様子 (C)種子の実体顕微鏡像 (D)種子の走査型電子顕微鏡像
栄養がないため、この種子は光合成をする通常の植物のように自力で発芽することができません。種子は風で運ばれた先で、偶然にも「正しいパートナー菌類(適合菌)」に出会う必要があります。
適合菌の菌糸が種子に侵入すると、初めて発芽に必要な栄養が供給され、プロトコルム(protocorm)と呼ばれる球状の幼生構造が形成されるのです。
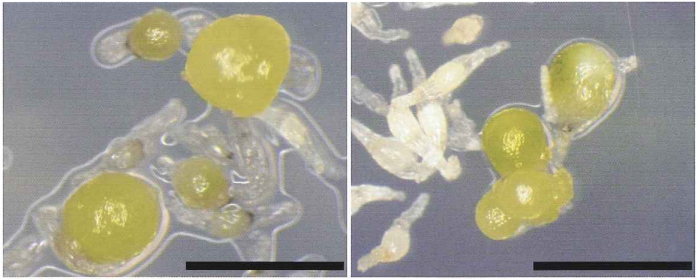

出典:島根県 ‐ キンセイラン及びナツエビネの種子発芽とその後の生育 春木 和久(2004年)
※左: キンセイラン (20℃で約3か月培養) 右: ナツエビネ (25℃で約3か月培養)
2022年の研究では、適合菌の土壌中での「存在量」が発芽成功率に直結することが示されました。つまり、適合する菌類がいる場所でしか種子は発芽できないため、菌従属栄養植物の分布は菌類の分布によって厳密に規制されています。



このため、菌従属栄養植物の多くは特定の林床微環境に限定され、希少種となる一因にもなっているのです。
このように、菌従属栄養植物は、
- 特定の菌類パートナーを化学シグナルで見極め
- 菌根菌ネットワークを通じて樹木から間接的に炭素を吸収し
- 菌類なしでは発芽すらできない種子構造を持つ
という、三つの巧妙で相互依存的な戦略によって生存しているのです。


森の見えない「つなぎ手」 ― 菌従属栄養植物が担う生態系での役割


出典:iNaturalist – Tianma Gastrodia elata
一見すると「ただ乗り」に見える菌従属栄養植物ですが、実は生態系全体を見ると、菌類や樹木との一方的な関係にとどまらない、多層的で重要な役割を担っています。主な役割を具体的に見ていきましょう。
地下ネットワークの健全性を示す指標生物
菌従属栄養植物が森の奥でひっそりと花を咲かせている姿。それは、足元の土の中で樹木と菌類のネットワークが健全に、そして複雑に結ばれていることの、何よりの「生きた証拠」です。
菌従属栄養植物はパートナーとなる菌類を厳しく選ぶ「究極の偏食家」です。特定の菌がいなければ生きていけない彼らがそこにいるということは、その地下に、私たちの目には見えないけれど豊かで精密な生態系が確実に息づいていることを証明しています。
保全生物学の観点からも、森の「菌根ネットワークの質」や「腐朽環境の健全性」を総合的に評価する「生物指標(バイオインディケーター)」として機能しています。代表的な生物指標となる種と、指標としての役割には以下のような例が挙げられます。
- ギンリョウソウ(Monotropastrum humile) ベニタケ属などの外生菌根菌(ECM)と、それが共生する健全な樹木(ブナ、マツなど)の存在を強く示唆します。ECMネットワークが成熟し、樹木と菌類の相互信頼が長年にわたって築かれている証です。
- ホンゴウソウ(Sciaphila spp.) 太古から続くアーバスキュラー菌根菌(AMF)のネットワークが、攪乱されずに残っている原生林に近い森の指標となります。極めて限定的な菌類依存性を示すため、その生育環境は特に貴重です。
- ツチアケビ(Cyrtosia septentrionalis) ナラタケなどの腐生菌が活発に働き、豊かな有機物が分解・循環している森の証です。朽木資源の豊富さと、腐朽菌の多様性が保たれていることを示します。
- キンラン(Cephalanthera falcata) 光合成もしながら菌類(ECM)にも頼る「部分的菌従属栄養植物」です。里山のような「明るさと暗さのバランスが取れた樹林環境」が保たれ、過度な伐採もなく適度な光が林床に届く環境の指標となります。
このような植物の有無を知ることは、単に「珍しい植物がいるかいないか」ではなく、その森全体の「命のネットワークの品質」を読み取ることです。菌従属栄養植物たちが息づく森は、地下から地表へと、見えない世界が確実に機能している、本当に豊かな森なのです。
小さな生き物たちへの栄養供給
菌従属栄養植物も、命をつなぐために花を咲かせます。その花は、暗い森の奥で暮らす小さな生き物たちにとって、貴重な食事の場としての役割を果たしているのです。
光の届かない林床には、ミツバチやチョウといった「いつもの顔ぶれ」はあまりやってきません。そこで菌従属栄養植物たちは、暗がりを好む特別なパートナーたちと手を結び、独自の「暗闇の送粉ネットワーク」を形成してきました。
日本の研究チームによって、その驚くべき関係が次々と明らかになっています。以下はその一部の例です。
クロヤツシロラン(Gastrodia pubilabiata )


出典:福岡県 ‐ 福岡県の希少生物 ‐ クロヤツシロラン(金光浩伸撮影)
クロヤツシロラン(Gastrodia pubilabiata )は、腐った果実のような匂いを漂わせ、キノコ食のフタオビショウジョウバエをおびき寄せます。この植物は受粉報酬として「腐った花びら」を提供し、ショウジョウバエに産卵場所と幼虫の食糧を同時に提供する「保育送粉(nursery pollination)」システムを進化させました。
また、夜行性蜂がデンプン豊富な疑似花粉(pseudopollen)を採集するシステムも備え、複数の送粉戦略で多様な昆虫を受け入れています。
ギンリョウソウ(Monotropastrum humile)


出典:iNaturalist – ギンリョウソウ(Monotropastrum humile) – (撮影 jodyhsieh)
ギンリョウソウ(Monotropastrum humile)は森の微小昆虫たちに蜜を提供し、彼らの体を花粉まみれにして運んでもらいます。純白の花は、暗い林床で生きる昆虫たちの目印となり、かつ重要な栄養源として機能しています。
タシロラン( Epipogium roseum )


出典:iNaturalist – タシロラン Epipogium roseum – (撮影者 loenjhih)
タシロラン( Epipogium roseum )は、薄暗い環境に特化した、特定のキノコバエやハナアブなどを主な送粉者として利用しています。この種も、暗い林床という極限環境での独自の進化戦略を示す例です。
さらに極端な例では、ツボミヤツシロラン(Gastrodia clausa )のように、花を咲かせることさえやめ、堅く閉じた蕾の中で自動的に受粉を完結させる「究極の閉鎖受粉(cleistogamy)戦略」をとる種もいます。この適応は、昆虫訪問が極めてまれな環境での究極の「自給自足戦略」を示しているのです。


出典:iNaturalist – Gastrodia clausa
このような植物は、光合成をやめた「変わり者」かもしれませんが、森の底で生きる小さな生き物たちにとっては、なくてはならない大切な栄養源として、生態系の循環をしっかりと支えているのです。菌従属栄養植物の花一つ一つが、森の地下と地表の暗い世界を結び、見えない命のネットワークを織りなす、極めて重要な結び目なのです。
菌類との進化的「駆け引き」
菌類にとって、光合成産物を返さない「ただ乗り」植物の存在は本来不利益です。そのため菌類は、栄養を渡さない相手を排除する防御メカニズムを進化させてきました。
一方、菌従属栄養植物はこの防御をすり抜けて栄養を得るための化学的戦略を磨いてきました。このような「防御」と「侵入」の静かな進化的駆け引き(共進化)は、互いの進化に影響を与え、森の地下における複雑な関係性を形作ってきたのです。



菌従属栄養植物の存在がなければ、菌類は「より効率的に栄養を配分する」という進化圧を受けず、現在ほど複雑で精密な防御メカニズムを発展させなかったかもしれません。
この複雑な相互作用が、結果として菌根ネットワーク全体の複雑性と堅牢性を高め、森林生態系全体の多様性と安定性に間接的に貢献していると考えられます。
物質循環への隠れた影響力
菌従属栄養植物は、単に腐生菌から栄養を「もらう存在」ではなく、むしろ「どの腐生菌を選別するか」によって、森林全体の炭素循環に微妙な調整をもたらす「舞台裏の調整者」として機能している可能性が指摘されています。菌従属栄養植物の「菌選別」は、朽木から放出される炭素が、いつ、どの速度で、どの経路を通って森全体へ配分されるかを制御する「地下の交通整理」としての役割を果たしているのです。
1. 分解速度の調整
菌従属栄養植物が依存する腐生菌の種類によって、落葉や朽木の分解速度が変わり、古い炭素が土壌に放出されるタイミングや量を左右します。例えば、ツチアケビが依存するナラタケ属(Armillaria)が活発に活動する林では、朽木の分解が加速され、古い炭素が通常なら60~100年以上かかるところを、20~30年単位で大気へ放出される傾向が示唆されています。
2. 炭素の「時間軸」制御
数十年~数百年単位で滞留していた炭素を再利用することで、炭素の循環期間を調整します。オニノヤガラ(Gastrodia elata)が依存する腐生菌が選別する朽木は、300年以上前のシイの木由来の古い炭素を利用する個体群も確認されており、極めて長期的な炭素再循環に関わっていることが実証されています。
3. 窒素環境への間接的影響
菌従属栄養植物が選別しやすいセルロース分解菌の活動が進むと、朽木内の窒素が消費され「窒素飢饉」状態が生まれます。この環境では、空気中の窒素を直接固定できる「窒素固定菌」の出番が増え、朽木全体の窒素バランスが変化するのです。
つまり、菌従属栄養植物の「菌選別」は、朽木内の窒素循環にも連鎖的に影響を与えているのです。
4. 土壌有機物の回転速度変化
菌従属栄養植物は、分解の加速や減速によって、長期的な土壌炭素の蓄積量に影響を与えます。ECM(外生菌根菌)優位環境ではサプロトロフ(腐生菌)が抑制され土壌炭素が蓄積しやすいのに対し、腐生菌依存型菌従属栄養植物が存在する環境では、腐生菌活性が高まり、土壌有機物の周転速度が加速される可能性が示唆されています。
5. 「炭素ゲート」機能
腐生菌が分解した炭素を菌従属栄養植物が利用することで、森全体へ炭素がどのように再配分されるかを制御する役割を果たします。朽木内の炭素が、いつCO₂として大気へ放出され、いつ土壌に保持され、いつ他の光合成植物へ再利用されるかは、菌従属栄養植物による「菌選別」の精密な調整を通じて決定されているのです。
これらの影響メカニズムは、2018~2025年の研究により段階的に示唆されているものですが、菌従属栄養植物による「調整度合い」の定量的評価には、さらなる長期的な生態系観測が必要です。しかし、これらの研究から見える共通点は、菌従属栄養植物が単なる「土壌の脇役」ではなく、森林の物質循環を支える「隠れた重要な調整者」である可能性が非常に高いということなのです。



一見菌類と通常の光合成する植物との共生ネットワークの「フリーライダー」のように見える菌従属栄養植物ですが、実はそれらのネットワークと別の生き物をつなぐ架け橋の役目もしていたのですね!
光合成に頼らないというユニークな生態的地位(ニッチ)を選択した菌従属栄養植物の存在は、実はその森の生物多様性を豊かにしているのです。


菌従属栄養植物の多様な世界 ― 代表種とその生態


出典:WIKIMEDIA COMMONS – Epipogium aphyllum plants
「菌従属栄養植物」と一口に言っても、その姿や生き方は驚くほど多様です。森の暗がりに透き通るように白くたたずむものから、光合成と菌類依存を巧みに使い分けるものまで、それぞれが独自の進化を遂げています。
この多様性は、単なる外見の違いではなく、生態戦略と進化系統の根本的な違いを反映しているのです。代表的な種と、その特徴を覗いてみましょう。
完全菌従属栄養植物 ― 光合成を完全に捨てた「森の白い幽霊」
完全菌従属栄養植物とは、葉緑素を完全に失い、生涯を通じて光合成を一切行わず、栄養のすべてを菌類に依存する植物たちです。「幽霊植物(Ghost plant)」や「幽霊蘭」とも呼ばれるこれらの植物は、太陽光が極めて少ない林床という極限環境の住人です。
その透明感のある色は、光の不足以上に、光合成システムを完全に放棄したという進化的な決断を象徴しています。これらの植物は光合成関連遺伝子がゲノムから大規模に欠失していることが分子系統解析によって確認されており、植物としては極めて特異な進化経路を示しています。
ツツジ科 Ericaceae ギンリョウソウ Monotropastrum humile


出典:iNaturalist – ギンリョウソウ Monotropastrum humile
- 和名: ギンリョウソウ(銀竜草)
- 別名: ユウレイタケ(幽霊茸)
- 学名:Monotropastrum humile (D.Don) H.Hara
- 分類: 被子植物門 双子葉植物綱 ツツジ目 ツツジ科 シャクジョウソウ亜科 ギンリョウソウ属
- 分布: 日本(北海道~沖縄)、ロシア(サハリン・千島列島)、朝鮮半島、中国、台湾、東南アジア(ベトナム、タイ、ラオス、ミャンマー)、ヒマラヤ(ネパール、ブータン、インド)
- 保護状況: 国際自然保護連合(IUCN)では評価なし。日本国内では絶滅危惧種指定なし(ただし一部地域では希少性が高い)。近縁種のM. kirishimenseは2022年記載の新種で、希少性が指摘されている
ギンリョウソウ(Monotropastrum humile)は、葉緑素を完全に失い、光合成をまったく行わない「完全菌従属栄養植物」の代表例です。森の林床の地下でベニタケ属(Russula)やチチタケ属(Lactarius)などの外生菌根菌と菌根ネットワークをつくり、その菌類が共生している樹木から、間接的に炭素や栄養をもらうことで生存しています。
透き通るような純白の茎と下向きに咲く筒状の白い花が、梅雨時(5月~8月)の湿った林床に現れる様は、「幽霊茸」と呼ばれるほど神秘的です。この姿は、光合成をしなくなったことにより不要になった葉緑素がないためです。
英語圏では近縁北米種のMonotropa uniflora が「Ghost Plant(幽霊植物)」や「Indian Pipe(インディアンパイプ)」と呼ばれており、ギンリョウソウ属全体が「見えない地下世界の住人」として世界的に認識されています。


出典:神戸大学 ‐ 世界でも2種目! 新種の「ギンリョウソウ」を発見(2022年11月30日)
2022年には、日本で従来ギンリョウソウ(Monotropastrum humile)の「色変異」と考えられていた赤みを帯びた個体群が、20年にわたる分子生物学的研究を経て、実は別種のキリシマギンリョウソウ(M. kirishimense )であることが発表されました。これにより、ギンリョウソウ属の多様性が従来の認識を上回ることが判明し、菌従属栄養植物の分類学的研究がなお進行中であることがよくわかります。
部分的菌従属栄養植物 ― 光合成と菌類依存を併用する「二重生活」
部分的菌従属栄養植物とは、自らも葉緑素を持ち光合成を行う一方で、菌類ネットワークからも栄養を得る、「二重生活」を送る植物たちです。光が少ない環境では菌類への依存度を高めるなど、極めて柔軟な栄養戦略をとります。
地上部は緑色を保つことが多く、通常個体と区別しにくい場合もあります。
ラン科 Orchidaceae キンラン Cephalanthera falcata


出典:WIKIMEDIA COMMONS – Cephalanthera falcata (top)
キンラン(Cephalanthera falcata)は、落葉広葉樹林の明るい林床に生える「部分的菌従属栄養植物」です。地上部の緑色の葉で光合成を行いながら、同時に地下で外生菌根菌(ベニタケ科、イボタケ科など)と共生し、必要な栄養の3~4割以上を菌からもらっています。
4月~6月に咲く鮮やかな黄金色の花が「金蘭」の和名の由来で、英語でも「Golden Orchid(ゴールデン・オーキッド)」と呼ばれています。
特定の菌根菌がいなければ生きられず、その菌類自体も豊かな樹林環境で樹木と共生する必要があるため、キンランが咲くことは里山の豊かな森の証となっています。近年の里山の手入れ不足や林床環境の変化により生育地が急速に減少し、絶滅危惧種として厳重に保護されています。
依存する菌の違い ― 地下ネットワークの多様性
菌従属栄養植物が依存する菌は、「共生する菌根菌の特徴」と「生きた樹木か死んだ有機物」かによって、生態学的に大きく3タイプに整理することもできます。
1️⃣ 外生菌根菌(EcM:Ectomycorrhizal fungi)依存型
外生菌根菌 (EcM)は、ブナ科(コナラなど)やマツ科といった樹木の根の外側を、菌糸の鞘(さや)で覆うように共生します。「キノコ」を作るものが多く、主に樹木から栄養(炭素)をもらう見返りに、窒素やミネラルを集めて渡します。
2024年の研究では、EcMと共生する樹木は風で受粉・散布する種が多いことが示されました。この密接で局所的なネットワークに侵入する外生菌根菌依存型の代表的な菌従属栄養植物はギンリョウソウ、キンラン、ベニバナイチヤクソウなどです。
ツツジ科 Ericaceae ベニバナイチヤクソウ Pyrola asarifolia subsp. incarnata


出典:iNaturalist – Pink Wintergreen Pyrola asarifolia ssp. incarnata
ベニバナイチヤクソウ(Pyrola asarifolia subsp. incarnata)は、緑色の丸い葉を持ち、自ら光合成を行うツツジ科イチヤクソウ属の常緑多年草です。6月~8月上旬に花茎に8~15個つく美しい桃色から濃桃色の下向き花が特徴で、英語では「Pink Wintergreen(ピンク・ウィンターグリーン)」や「Rosy Pyrola」と呼ばれています。
暗い林床や冷涼環境でも生育するため、光合成だけでは賄えない栄養を地下の菌類ネットワークから補う「部分的菌従属栄養植物」であることが、安定同位体解析で確認されています。ベニバナイチヤクソウが依存するパートナー菌は、ベニタケ科などの外生菌根菌(ECM)の仲間です。
元来北方系の分布を持つ種ですが、日本国内での分布は限定的で、特に分布南限にあたる近畿地方では極めて希少です。生育地の消失や気候変動による環境変化にさらされています。
また、光合成能を持ちながらも菌根菌への依存を深めてきた、進化の途上にある貴重な存在として注視されています。
2️⃣ アーバスキュラー菌根菌(AMF:arbuscular mycorrhizal fungi)依存型
アーバスキュラー菌根菌 (AMF)は、地球上の植物の8割以上が利用する、最も古く広範なネットワークです。植物の根の細胞内部にまで菌糸を侵入させ、「樹枝状体」と呼ばれる器官を作って栄養交換を行います。
AMFは主に、植物が集めにくいリン酸を渡す役割を担っています。ホンゴウソウ科、ヒナノシャクジョウ科の一部などのアーバスキュラー菌根菌依存型の菌従属栄養植物は、この広大で多様なネットワークに依存しています。
2024年の研究では、AMFと共生する樹木は動物に受粉・散布を頼る種が多いことが示されました。
ホンゴウソウ科 Triuridaceae オモトソウ Sciaphila sugimotoi


出典:神戸大学 ‐ 新種の光合成をやめた植物を石垣島で発見(2017年7月25日)


出典:末次 健司,他 ‐ オモトソウ(ホンゴウソウ科)を西表島に記録する(2021年)
オモトソウ (Sciaphila sugimotoi )は、2017年に石垣島の於茂登岳で発見・記載された、光合成を完全にやめた「完全菌従属栄養植物」です。「アーバスキュラー菌根菌」という、広範な菌類ネットワークに依存し、そのネットワークを通じて周囲の光合成できる植物からの栄養を間接的に奪い取っています。
地上部の高さはわずか5~10cm程度で、直径2mm前後の紫色の小さな花をつけます。雄花の花被片6枚すべての先端に球状の付属体をつける点が、3個の付属体をつける同属のホンゴウソウ (Sciaphila nana)との重要な識別ポイントです。



ホンゴウソウはこちら👇️


出典:iNaturalist – ホンゴウソウ Sciaphila nana
発見から間もないため、現在確認されているのは石垣島と西表島、そして台湾の蘭嶼の限定的な地域のみで、西表島では約20個体のみ確認されており、個体数も極めて少なく、森林伐採と局地的な環境変化に対して非常に脆弱です。ホンゴウソウの発見は、熱帯地域における菌根ネットワークの複雑さと、その中で進化した多様な菌従属栄養植物の存在を示す、生物学的に重要な証拠です。
3️⃣ 腐生菌(saprotrophic fungi)依存型
腐生菌(saprotrophic fungi)は、生きた樹木とは共生せず、枯れ木や落ち葉などの死んだ有機物を分解して栄養を得る菌です。外生菌根菌(ECM)やアーバスキュラー菌根菌(AMF)が「生きた樹木との相利共生」を基本とするのに対し、腐生菌は「有機物の一方的な分解」が役割であり、純粋に分解者として機能しています。
腐生菌依存型の菌従属栄養植物は、光合成できない樹木の「新しい栄養」ではなく、腐生菌が分解した朽木由来の「古い炭素」を利用しています。つまり、彼らは「過去に樹木が固定した光合成産物」を、数十年~数百年のタイムラグを置いて間接的に利用しているのです。
この戦略により、生きた樹木が存在しない環境でも生存でき、より独立した生態的ニッチを獲得しています。ただし、安定した腐朽環境(湿度・温度)が必須であるため、分布は限定的です。
腐生菌依存型の菌従属栄養植物として代表的なのは、ツチアケビ、オニノヤガラの一部などです。
ラン科 Orchidaceae ツチアケビ Cyrtosia septentrionalis


出典:WIKIMEDIA COMMONS – Cyrtosia septentrionalis (Montage)
ツチアケビ(Cyrtosia septentrionalis )は、光合成を完全にやめた「完全菌従属栄養植物」のラン科植物で、地下で木材を分解する強力な腐生菌であるナラタケ属(Armillaria)と共生し、そこからすべての栄養と炭素を得ています。高さ30~170cm(通常40~90cm)の茎は淡黄色で、6月~7月に黄緑色の花を咲かせた後、秋に鮮やかな赤色の実をつけます。
この赤い実がアケビの実に似ていることから「土のアケビ」という和名がついたとされ、英語では「Red Sausage Orchid(赤いソーセージのラン)」と呼ばれることもあります。学名の「septentrionalis」は「北方」を意味し、熱帯から温帯アジアに分布するツチアケビ属5種の中で、この種が最も北に分布する種であることを示しています。
森林環境の変化、特に落ち葉層の喪失や林の皆伐、気候変動によるナラタケの衰退が、ツチアケビの個体群を急速に減少させており、保全の重要な対象種となっています。
菌根の「構造」による細分化された分類
生態的な役割による分類とは別に、菌類が植物の根にどのように接続しているか、その「構造(形態)」に注目すると、菌根はさらに細かく7つのタイプに分類されます。同じ菌従属栄養植物でも、この構造レベルでは異なる分類になることがあります。
- アーバスキュラー菌根: 根の細胞内に樹枝状体を形成。AMFに特有。最も広範に分布。
- 外生菌根: 根の外側を菌糸の鞘で覆う。ECMに特有。マツ科やブナ科など特定の樹木に限定。
- 内外生菌根: 外側の鞘と内部への侵入の両方の特徴を持つ。進化的な過渡段階の可能性も。
- エリコイド菌根: 根の細胞内でコイル状になる。ツツジ科の一部やエリカなど、酸性土壌に生育する植物に特有。
- アーブトイド菌根: 鞘と細胞内のコイル構造の両方を持つ。複合型の特性を示す。
- モノトロポイド菌根(シャクジョウソウ型): 根の細胞に杭を打ち込むように菌糸が侵入。ギンリョウソウなど一部の腐生菌依存型に特有。
- ラン菌根: 根の細胞内で菌糸の塊(ペロトン)を形成。ラン科植物全般に特有で、ラン科の菌従属栄養植物もこの構造。
菌従属栄養植物は複数回独立に進化し、同じ科の中でも異なる菌類パートナーを選ぶことがあります。最新研究では、同じ種でも地域や個体群ごとに異なる菌類を利用する場合があることが確認されており、菌依存度も「部分的」から「完全」まで連続的に変化します。



とにかく多様で複雑なのですね!
菌従属栄養植物は、その依存度やパートナーとする菌類の種類によって、実に多様な生き方を実現しているのです。完全から部分的へ、外生から内生へ、腐生菌から共生菌へ…。
これらの多様な選択肢は、進化が生み出した、環境への適応の多様性を象徴しています。このような植物の存在は、地上のバイオーム以上に、地下のネットワークが生態系の豊かさを支えていることを、静かに物語っているのです。


菌従属栄養植物の最新研究 ― 解明される進化と共生の謎


出典:Phytotaxa – Gastrodia motuoensis (Orchidaceae, Epidendroideae), a new species of mycoheterotrophic plant from Xizang, China, based on morphological and molecular evidence(2025年7月)
かつては「森の隠れた存在」として目立たぬ扱いを受けてきた菌従属栄養植物。しかし近年、次世代シーケンサーなどの分子・生態学的な革新的技術により、謎に満ちていた進化と共生の仕組みが、ゲノムレベルから生態系レベルまで、次々と明かされつつあります。
そこで見えてきたのは、従来の植物進化の常識をはるかに超える現象の数々です。
驚異的なゲノム縮小と遺伝子喪失のメカニズム ― 寄生植物を超える極限
光合成をやめた彼らの進化は、単なる「機能の停止」ではありませんでした。最新のゲノム解析が描き出したのは、生きるために不要なものを徹底的に削ぎ落とす「究極のミニマリスト」としての姿です。
オニノヤガラ(Gastrodia elata )などの完全菌従属栄養植物では、植物の設計図である葉緑体ゲノムが、一般的な植物の約7~10分の1に圧縮されています。光合成を行うための酵素群はもちろん、光を感じるセンサーや、複雑な根や葉を発達させるための遺伝子まで、必要がないからと次々と削除されているのです。
寄生植物が宿主から遺伝子を「奪う」ことで複雑化するのとは対照的に、菌従属栄養植物は「持たないこと」を戦略的に選びました。暗い地下で、特定の菌類というパートナーに生存を完全に委ねる…。その潔い決断が、無駄を極限まで省いた、美しく驚異的な引き算の進化を生み出したのです。
この削減戦略は、決して「退化」ではなく、極限環境への最適化という、生命のしたたかな創意工夫なのです。菌従属栄養植物たちが選んだ「シンプルさ」は、実はとても複雑な環境適応の結果——つまり、不要なものを完璧に削り落とすことで、ただ一つの必要なもの(菌類との関係)に特化した、究極の戦略的進化なのです。
相手との関係の違いが、進化を分ける ― 直接接触 vs. 間接ネットワーク
寄生植物と菌従属栄養植物は、どちらも「他者に頼る生き方」を選びました。しかし、その結果は全く異なっています。
- 寄生植物(ネナシカズラやハマウツボなど)の戦略
相手の植物に直接「吸器」という器官で取り付き、相手の組織に侵入します。この直接接触の過程で、寄生植物は宿主植物の遺伝子そのものを奪い取る「遺伝子水平伝播」※という現象が起きます。
つまり、相手を支配することで、相手の強力な遺伝子を自分たちに組み込んでしまうのです。 - 菌従属栄養植物の戦略
菌類という仲介役を挟むため、決して宿主植物に直接触れません。菌を通じて栄養を受け取るだけです。最新研究では、菌従属栄養植物のゲノムにおいて、寄生植物ほど多くの「遺伝子水平伝播」が起きていないことが判明しました。
つまり、相手の遺伝子を奪わず、代わりに自分の不要な遺伝子を削除することで、進化を遂行しているのです。
同じ「依存する生き方」でも、相手との接触方法(直接 vs. 間接)が、進化の道筋を全く変えてしまう…。この違いは、生命の多様な戦略性を示す、極めて興味深い事例なのです。
遺伝子水平伝播🧬
遺伝子水平伝播(いでんしすいへいでんぱ)とは、遺伝子が親から子へ「垂直」に伝わる(遺伝)のとは違い、個体間や異なる種の間で「水平」にコピー&ペーストされる現象です。つまり、遺伝子の鋳型が他の生物に直接移され、機能する、という極めて異例な進化メカニズムなのです。
特に細菌(バクテリア)の世界では日常的に行われており、細菌はこの現象を通じて、他の細菌や異なる微生物から有用な遺伝子を「借用」しています。これが、抗生物質が効かなくなる「耐性遺伝子」を仲間同士で交換し合う主な手段となり、医療現場では「スーパーバグ(超耐性菌)」が急速に蔓延する深刻な問題を引き起こしています。
ヘビからカエルへの遺伝子水平伝播
2024年、日本の研究チームが驚くべき発見を報告しました。ヘビに特徴的な「BovB」という動く遺伝子が、被食者であるカエルに飛び移っていたのです。通常、捕食者から被食者への遺伝子移動など考えられませんが、この現象は世界中で少なくとも42回起きており、特にマダガスカルでは過去5,000万年間に14回以上も発生しています。


出典:広島大学 ‐ 【研究成果】ヘビの遺伝子がカエルに飛び移る?−寄生虫が仲介する遺伝子水平伝播のパンデミック−(2022年4月)
研究により、この仲介者はヘビとカエルの両方から吸血する寄生虫(ヒルなど)であることが判明しました。寄生虫が「遺伝子の運び屋」として機能し、異なる動物間で遺伝子を媒介しているのです。
さらに興味深いのは、アフリカからマダガスカルに移住したカエルが、移住後に初めてこの遺伝子を獲得したことです。これは人間がマラリアに感染した地域に移住する仕組みと極めて似ており、高等動物間の遺伝子水平伝播が風土病と同じメカニズムで広がる可能性を示唆しています。
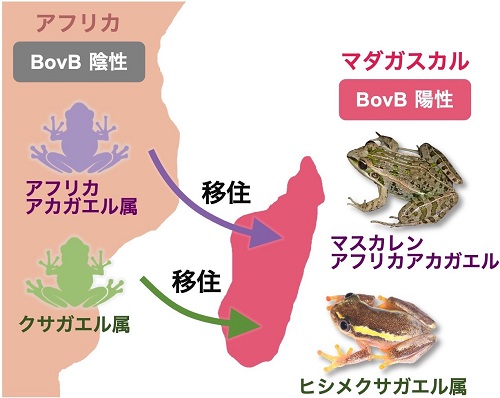

出典:広島大学 ‐ 【研究成果】ヘビの遺伝子がカエルに飛び移る?−寄生虫が仲介する遺伝子水平伝播のパンデミック−(2022年4月)
細菌にとっては、突然変異を待たずに急速に進化できる強力なメリットですが、人類にとっては医療や農業上の大きな脅威となります。一方、
- 寄生植物ラフレシアが吸器を通じて宿主から遺伝子を盗む
- アブラムシが菌類から色素合成に必要な遺伝子を獲得
- 苔が水中から陸上へ進出する際に原核生物から重要な遺伝子を受け取る
など、生物の進化に大きな影響を与える現象として注目されています。
これは、進化は「親から子へ」という垂直の流れだけでなく、「種を超えた水平の流れ」によっても形作られているという、従来の進化論を書き換える発見なのです。
参考・引用
理化学研究所 ‐ イネ科の宿主から寄生植物へ、核内遺伝子が水平伝播する現象を発見-寄生植物が、栄養源に加えて遺伝子も宿主植物から獲得-(2010年5月)
松井 一彰 ‐ 微生物生態系における細菌の遺伝子水平伝播現象(2015年8月)
Wikipedia – Horizontal gene transfer
Nature Communications – Widespread impact of horizontal gene transfer on plant colonization of land
EBSCO Research Starters – Lateral gene transfer
PMC (PubMed Central) – Lateral gene transfer between prokaryotes and eukaryotes
PMC (PubMed Central) – Horizontal gene transfer between bacteria and animals
Royal Society Publishing – Horizontal gene transfer in evolution: facts and challenges
同位体トレーサーが描く「栄養の地図」 ― 時間を超えたネットワークの流動
菌従属栄養植物がどこから栄養を得ているのか。最新の同位体解析技術は、その答えを「地図」として描き出しました。
これまでの同位体解析は、「菌従属栄養植物と樹木がつながっている」という事実を証明することが目的でした。しかし近年では、「どの樹木から、どの菌を経由し、どれくらいの栄養が流れているのか」という、栄養の詳細な流れを追跡できるようになったのです。
菌の種類で、栄養源の「時間軸」が変わる
腐生菌に依存する種(オニノヤガラなど)の菌従属栄養植物は、「数十年~数百年前に朽木に蓄えられた古い炭素」を利用しています。一方、外生菌根菌に依存する種は、「樹木が最近つくった新しい炭素」を得ています。つまり、菌従属栄養植物たちは、菌の種類によって、過去と現在の資源を使い分けながら森全体から栄養を吸収しているのです。
この「新旧の炭素を巧みに利用する戦略」は、森の長期的な炭素循環を理解する上で、極めて重要な手がかりをもたらしています。菌従属栄養植物は単なる「栄養の受け手」ではなく、地下で複雑に絡み合った時間軸まで含むネットワークの一部として機能しているのです。
共生方式の違いが生む進化的分岐 ― ECM型とAMF型の樹木戦略
2024年の京都大学の研究により、菌従属栄養植物が選ぶ「菌のタイプ」は、実はその森の樹木がどのように進化してきたか(風で運ばれるか、動物に運ばれるか)と深く結びついていることが分かってきました。
外生菌根菌(ECM)依存型と樹木の進化パターン
菌従属栄養植物の例: ギンリョウソウ、キンラン、ベニバナイチヤクソウなど
ECM樹木の特徴: ブナ科(ブナ、コナラ、クヌギなど)やマツ科(アカマツ、クロマツなど)の樹木は、外生菌根菌と共生し、親株周辺で同種の幼苗の生育を促進する「正のフィードバック効果」を示します。この効果により、樹木は密集して成長し、種子は主に風や重力による短距離散布を行い、花粉も風媒受粉に依存する傾向があります。
アーバスキュラー菌根菌(AMF)依存型と樹木の進化パターン
菌従属栄養植物の例: オモトソウなどホンゴウソウ科、ヒナノシャクジョウ科の一部
AMF樹木の特徴: 地球上の被子植物の約80%と共生するAMFは、親株周辺で同種の幼苗の生育を阻害する「負のフィードバック効果」を示します。病原菌や植食者が蔓延しやすいため、樹木は種子を親株から離れた位置に散布する必要があり、動物による長距離種子散布と動物媒花粉(昆虫や鳥類による受粉)を進化させました。
代表的な樹木として、ウワミズザクラ、オオカメノキ、ヤマボウシ、クサギなどが挙げられます。
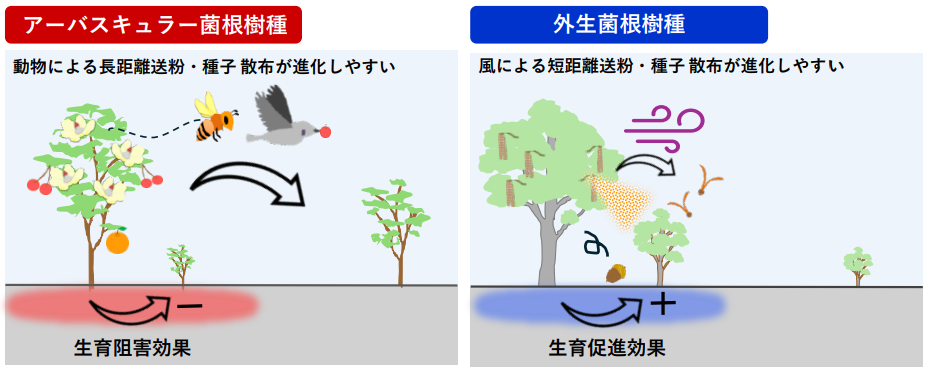

出典:京都大学 ‐ 世界各地、1 万種の解析から見えてきた樹木の進化パターン―送粉共生、種子散布共生、菌根共生の相関進化―(2024年5月10日)
ゲノムレベルから生態系レベルまで、最新科学が次々と明かしつつある菌従属栄養植物の驚異的な実態。その研究は、単に珍しい植物の謎を解くにとどまらず、進化研究・生態系保全・気候変動対策という、21世紀生物学の三つの重要課題に架け橋をかける存在として機能しています。
菌従属栄養植物の研究を通じて、生命の想像を超える創造性と、森全体の「見えない複雑さと豊かさ」が、いま改めて見直されているのです。


森の「見えないつながり」が教えてくれること ― 生命の多様性と共生の価値


出典:iNaturalist – Rhizanthella gardneri
※地下で花を咲かせる(完全地中生)珍しいラン
森の奥深く、光の届かない林床で静かに生きる菌従属栄養植物。これらの植物は「光合成を捨てる」という大胆な進化的選択をし、地下の菌類ネットワークに命を託しています。
一見「ただ乗り」とも見える生き方ですが、実は暗い森を生き抜くための究極の適応戦略であり、森全体に広がる目に見えない複雑なつながりと、生命の多様な知恵を私たちに伝えてくれています。2025年には、世界の菌根菌多様性ホットスポットの大半が保全区域外にあると警告する最新マップが発表され、地下ネットワークの保全が生態系持続の鍵であることが、科学的にも明らかになりました。
豊かな森(菌類ネットワーク)の指標としての存在
菌従属栄養植物は、特定の樹木と菌類が健全につながる森でしか生存できず、その存在は地下菌根ネットワークという「見えない基盤」が正常に働いている証しです。2024年の研究では、耕作地から再生した森に菌従属栄養植物が再登場することが、生態系回復の有力なサインになると実証されています。
反対に、もしこれらの植物が消え始めたら、それは森の健康が崩れ始めた「早期警告」とも言えるでしょう。
「寄生」と「菌従属栄養」 ― 光合成をやめた植物たちの二つの道
光合成を放棄した植物には、他の植物に直接取り付き遺伝子さえ奪う「寄生型」(ネナシカズラなどの寄生植物)と、菌類を仲介役とする「菌従属栄養型」(今回紹介した菌従属栄養植物)の二つの道があります。前者は「直接接触」、後者は「間接ネットワーク」という明確な違いがあり、進化の軌跡自体を大きく分けました。
それぞれが達した究極の適応からは、生命が選ぶ多様な答えの一部を垣間見ることができます。
生命の多様な戦略 ― 競争・寄生・共生の織りなす世界
生物の関係は「競争」か「共生」という単純で直接的な二択ではなく、例えば「森」という環境を包括的に見ると、菌従属栄養植物は多層的な役割を持ちます。たとえば、これらの植物は送粉昆虫に食料を提供し、菌類・樹木・他の植物との関係を調整する隠れたキープレイヤーです。
2025年の研究発表では、部分的菌従属栄養のラン科植物が菌類由来の栄養で繁殖成功率を高めていることも確認され、地下ネットワークの価値が一層強調されました。こうしたネットワークは、生物多様性と生態系レジリエンスの支えでもあります。
目に見えなくても大切なものがある…。その気付きこそが、森も社会も、未来の多様性ある幸福へ導く第一歩です。
すべての生命が複雑につながり合い、壮大な循環の中で共生している地球社会には、まだまだ私たちの知らない側面が隠されているでしょう。これからも素敵な地球のパズルのピースを、皆さまと共有できたら幸いです。
植物が好きな人には、こちらもおすすめ👇️


おまけ : 観察に出かけよう!





実際に菌従属栄養植物を探してみましょう!
菌従属栄養植物たちは、光合成をする必要がないため、普段は地下で菌類と静かに共生しています。彼らが地上で私たちの目に触れるのは、子孫を残すための「花」を咲かせ、「種子」をつくる、ごく限られた期間だけです。特に梅雨前後の初夏(5月下旬~7月中旬) は、複数の種が一度に地上に現れる絶好の観察シーズンになります。
季節ごとの主な開花時期



地域や場所、標高等によって、観察できる時期やタイミングは少しづつ違います。目的の植物、または行く場所にあわせて、事前に調べてから出発しましょう。
春(4月~5月)
部分的菌従属栄養植物たちが活動を始めます。美しい黄色の花を咲かせるキンラン(Cephalanthera falcata)や、緑色の花が特徴的なシュンラン(Cymbidium goeringii)が見頃を迎えます。
梅雨の時期(5月~7月)
「幽霊植物」の代表格、ギンリョウソウ(Monotropastrum humile)が活躍する季節です。雨上がりの湿った林床で、その透き通るような純白の姿が最も美しく見えます。同時期に、複数のギンリョウソウ属やエピポジウム属も花を咲かせ、林床に小さな白い世界が広がります。
夏~秋(6月~9月)
オニノヤガラ(Gastrodia elata)やマヤラン(Cymbidium macrorhizon)といった、より大型の菌従属栄養植物が花茎を伸ばし始めます。特にマヤランは初夏と秋の二度にわたって開花する珍しい種で、見かけたら幸運です。
出会うための観察のコツ



ただでさえレアな植物なので、できる限り出会える確率の高い場所とタイミングを狙いましょう。装備を整え、条件の良い森に何度も足を運んでみてください。
探すべき環境
樹齢が古く、コナラやカシ類などの広葉樹に覆われた林で、厚い落葉層がある場所を選びましょう。こうした環境には、菌従属栄養植物を支える菌根菌ネットワークが良く発達しています。
観察のベストタイミング
雨上がりの朝や湿度の高い日中は、白い花がより鮮明に見え、キノコバエなどの送粉昆虫も活動しているため、撮影の好機です。また、こうした時期には菌類も活発に動いており、森全体の豊かなエコシステムの一部を目撃できるでしょう。
足元への配慮
道沿いからあまり踏み込まず、林床の生き物や土壌に気をつけながら、慎重に探してみてください。菌従属栄養植物は根が浅く、土を踏み固めるだけでも大きなダメージを受ける可能性があります。



夢中になって地面を探していると、いつの間にか深入りしてしまったり、思わぬ怪我をしたりすることもあります。森という聖域に「お邪魔させてもらう」という謙虚な気持ちで、安全には十分に配慮しましょう。
服装・持ち物など
菌従属栄養植物が暮らすのは光の届かない森の奥深く、そして観察のベストシーズンである梅雨時は、足元が滑りやすく、蚊やマダニ、地域によってはヤマビルなどの吸血生物も活発になる時期です。
ここでは、初心者の方でも安心して探索でき、かつ観察をより楽しむための、身を守るための装備と、アイテムをまとめました。
身を守るための服装
- 長袖・長ズボン:虫刺されや植物によるかぶれ、擦り傷を防ぐため、季節を問わず肌の露出は控えましょう。
- 防水トレッキングシューズまたは長靴:湿った林床は非常に滑りやすくぬかるんでいるため、足首を保護できる防水の靴が安心です。
- 帽子:頭上からの落下物や髪の毛への虫の侵入、直射日光を防ぎ、転倒時の頭部保護にもなります。
- レインウェア(雨具):山の天気は変わりやすく、雨上がりの濡れた藪を歩く際の防水と防寒に役立ちます。
観察と安全のための必携持ち物
- 虫よけスプレー・ヤマビル対策:蚊やダニ、地域によってはヤマビル対策の忌避剤や塩水を持参すると効果的です。
- ルーペ(10倍程度):菌従属栄養植物の花は数ミリと極めて小さいため、ルーペがあると肉眼では見えない繊細な構造や美しさが見えてきます。
- ヘッドライト・懐中電灯:林床は昼間でも薄暗いため、ライトがあると隠れた花を見つけやすくなります。
- カメラまたはスマートフォン:採集は厳禁です。美しい姿は「摘まずに撮る」ことで、記憶とデータに残して持ち帰りましょう。
- 地図・GPSアプリ:地面に夢中になると方向感覚を失いやすいため、現在地を確認できる手段は必須です。
- 園芸手袋:倒木や苔むした岩に触れる際、汚れや怪我、有毒生物との接触を防ぎます。
- 熊鈴:地面に集中していると周囲への注意が散漫になりがちです。野生動物にこちらの存在を知らせるために携行しましょう。
- 救急セット:万が一の小さな怪我や虫刺されに備え、絆創膏、消毒液、虫刺され薬などを準備しましょう。
- 飲料水と補給食:長時間の探索時の疲労回復と熱中症予防に必要です。
重要なお願い ― 「見守る」ことの大切さ
これらの植物の多くは、特定の菌類との繊細なバランスの上でようやく生きている、極めて希少な存在です。もし幸運にも出会えたら、採集や掘り返し、踏みつけは絶対にしないでください。
菌従属栄養植物は菌のネットワークなしでは生きられないので、写真に記録するなど、そっと見守ることが大切です。また、遊歩道や登山道などから、むやみに外れて踏み入らないように心がけ、繊細な森の循環とネットワークを大切にしながら観察しましょう。



素敵な生き物に出会えたら、そっと観察・記録して、また次の機会、次のシーズンに会えることを願いましょう!
生き物全般が好きな人には、こちらもおすすめ👇️





【広告】この記事は「SWELL」というWordPressテーマで執筆しています。有料ですが買い切りなので、長く快適にブログを続けたい人にはおすすめですよ!👇️


参考・引用
「菌従属栄養植物」とは ― 菌類のネットワークに頼る生き方
New Phytologist – The biology of myco‐heterotrophic (‘saprophytic’) plants
Annals of Botany – Myco-heterotrophy: when fungi host plants
神戸大学ニュースサイト – 枯れ木を食べる植物「腐生植物」は存在するのか!?
菌従属栄養植物 研究の歩み ― 謎に満ちた生態の解明史
Science Direct – Mycoheterotrophy: An overview of historical and current research
Genome Biology and Evolution – Lineage-Specific Reductions of Plastid Genomes in an Orchid Tribe
神戸大学 – 枯れ木を食べる植物「腐生植物」は存在するのか!?
DTIC – The Role of Mycorrhizal Fungi in Ecosystem Energetics
PMC – Phylogenetic position and plastid genome structure of Corsiaceae
Frontiers in Plant Science – Genome Skimming Reveals Plastome Conservation in Calypso
なぜ「菌類依存」という道を選んだのか? ― 進化の背景
神戸大学 ‐ なぜ寄生を選ぶ植物が存在するのか?光合成の代わりに菌に依存する生活の意義を解明(2025年2月)
日本植物学会 ‐ 光合成をやめた植物ー菌従属栄養植物のたどった進化の道のり(2014年)
日本植物学会 ‐ 菌従属栄養性の生活様式を可能にした様々な適応進化ー特に送粉様式の変化について(2014年)
Genome Biology and Evolution – Lineage-Specific Reductions of Plastid Genomes in an Orchid Tribe
東京大学 ‐ 共生微生物による植物生長促進機能や植物保護機能を支える分子基盤の理解
Science Portal ‐ 不利な進化はどうして? 光合成をやめる途中段階の藻類を発見 国環研(2022年2月)
菌従属栄養植物の「戦略」 ― 菌類ネットワークへの侵入から繁栄まで
Science Direct – Mycoheterotrophy: An overview
Nature – Evolutionary histories and mycorrhizal associations of mycoheterotrophic plants (2021年4月)
Botanical Briefing – Strigolactones: Chemical Signals for Fungal Symbionts (2006年)
千葉大学 – 菌類・きのこを食べる「菌従属栄養植物」の菌根共生系の解明 (201710月年)
神戸大学 ‐ 共生菌に栄養を依存するラン (蘭) の発芽メカニズムを解明 発芽促進剤を用いた絶滅危惧種の保全へ(2023年10月)
Nature Plants – Mycoheterotrophy in the wood-wide web(2024年4月)
森の見えない「つなぎ手」 ― 菌従属栄養植物が担う生態系での役割
University of Bayreuth – Mycoheterotrophic plants as a key to the “Wood Wide Web”
PubMed Central – Secondary Metabolites in Nectar-Mediated Plant-Pollinator Relationships(2023年1月25日)
神戸大学 ‐ 枯れ木を食べる植物「腐生植物」は存在するのか!?大気圏核実験由来の放射性炭素同位体を用いた新たな検証(2020年1月24日)
名古屋大学 ‐ 光合成機能喪失の進化メカニズム(2025年7月1日)
チバニアン兼業農学校 ‐ 従属栄養細菌の秘密に迫る(2023年7月1日)
菌従属栄養植物の多様な世界 ― 代表種とその生態
Botany One – The genetic prison that traps a ghost plant(2025年6月)
Science Daily – Ethereal color variant of mysterious plant is actually a new species(2022年12月)
Kew Royal Botanic Gardens – Ghost plant (Monotropa uniflora)
Mycorrhizas.info – Ectomycorrhizal Fungi
菌従属栄養植物の最新研究 ― 解明される進化と共生の謎
New Phytologist – Genome evolution in plants and the origins of innovation(2023年9月2日)
BioRxiv – Plastid genome evolution in leafless members of the orchid family(2023年11月3日)
The Wire Science – The Mysterious Plants That Thrive in Darkness and Steal Food(2019年8月22日)
森の「見えないつながり」が教えてくれること ― 生命の多様性と共生の価値
Nature – Global hotspots of mycorrhizal fungal richness are poorly protected (2025年7月23日)




コメント